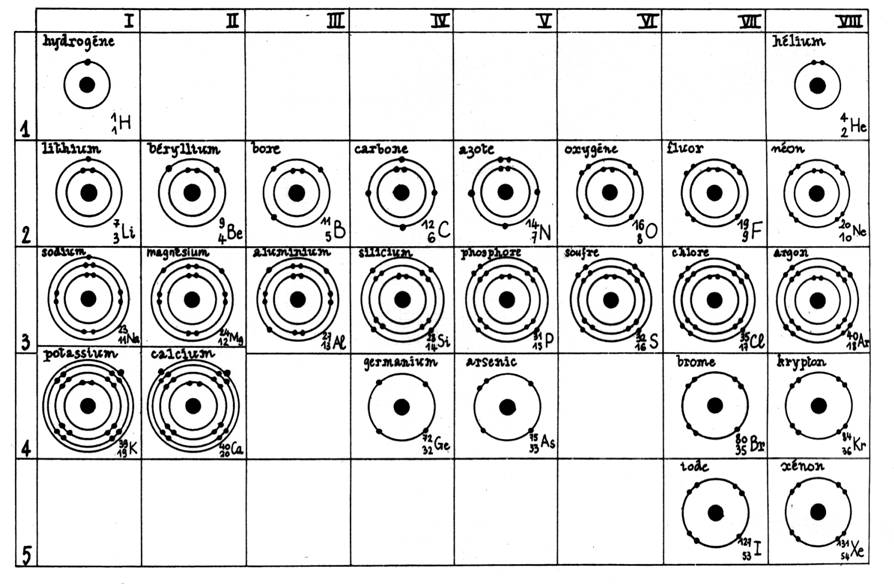
Extrait du
tableau des classifications des éléments chimiques
(représenté avec le modèle de Bohr ) :
Premières analyses : le nombre en bas à gauche
est appelé « nombre atomique »
Nous constatons que les éléments peuvent être
classés par ordre de nombre atomique croissant.
Remarquons qu’au remplissage d’une couche
électronique ( niveau d’énergie) correspond à une « période »
(ligne)
|
|
On admettra :
Les éléments de la première colonne ( lithium, le
sodium et le potassium) ont la même réaction chimique ( apparition d’une flamme
en contact avec l’eau)
Les éléments appartenant à la dernière colonne sont
appelés « gaz rares » ou « gaz inertes » . Ils sont
très peu réactifs chimiquement. La couche électronique externe est saturée. La
présence de huit électrons (deux pour la
première couche, sur la couche externe) explique la faible réactivité chimique.
Pour les éléments des autres colonnes (compris
entre la première et la dernière colonne) , c’est au cours d’une réaction
chimique qu’ils vont évoluer vers la stabilité en saturant leur couche électronique externe.